Page 114 - 11-kimya-beceri-temelli-soru
P. 114
3) Donma Noktası Alçalması (Kriyoskopi)
Saf suda ucucu olan sıvılar ya da uçucu olmayan katılar çözüldüğünde oluşan çözeltilerin donma noktası saf
çözücünün donma noktasından daha düşüktür. Çözeltinin derişimi arttıkça donma noktasındaki düşme miktarı
artar.
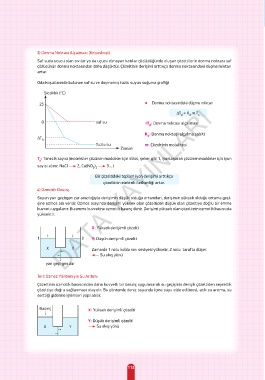
Oda koşullarında bulunan saf su ve doymamış tuzlu suyun soğuma grafiği
Sıcaklık (°C)
25 ● Donma noktasındaki düşme miktarı
DATA YAYINLARI
DT = K .m.T s
d
d
0 saf su DT : Donma noktası alçalması
d
K : Donma noktası alçalma sabiti
DT k d
Tuzlu su m: Çözeltinin molalitesi
Zaman
T : Tanecik sayısı (moleküler çözünen maddeler için alkol, şeker gibi 1, iyonlaşarak çözünen maddeler için iyon
s
sayısı alınır. NaCl 2, Ca(NO ) 3... )
3 2
Bir çözeltideki toplam iyon derişimi arttıkça
çözeltinin elektrik iletkenliği artar.
4) Ozmotik Basınç
Suyun yarı geçirgen zar aracılığıyla derişimin düşük olduğu ortamdan, derişimin yüksek olduğu ortama geçi-
şine ozmos adı verilir. Ozmos olayında derişimi yüksek olan çözeltiden düşük olan çözeltiye doğru bir emme
kuvveti uygulanır. Bu emme kuvvetine ozmotik basınç denir. Derişimi yüksek olan çözeltinin ozmotik basıncıda
yüksektir.
X: Yüksek derişimli çözelti
1 2 Y: Düşük derişimli çözelti
X Y Zamanla 1 nolu kolda sıvı seviyesi yükselir, 2 nolu tarafta düşer.
Su akış yönü
yarı geçirgen zar
Ters Ozmoz Yöntemiyle Su Arıtımı
Çözeltinin ozmotik basıncından daha kuvvetli bir basınç uygulanarak su geçişinin derişik çözeltiden seyreltik
çözeltiye doğru sağlanması olayıdır. Bu yöntemle deniz suyunda içme suyu elde edilmesi, atık su arıtma, su
sertliği giderme işlemleri yapılabilir.
Basınç X: Yüksek derişimli çözelti
Y: Düşük derişimli çözelti
X Y Su akış yönü
112